Ремиссия психоза у пациента с резистентной шизофренией после трансплантации костного мозга: описание клинического случая
(Перевод публикации Remission of Psychosis in Treatment-Resistant Schizophrenia following Bone Marrow Transplantation: A Case Report
Департамент психиатрии, Медицинский институт, Университет Симане, Идзумо, Япония
В данной работе нами представлен клинический случай 24-летнего пациента-мужчины, страдавшего резистентной шизофренией с преобладанием тяжелой бредовой симптоматики и галлюцинаций и перенесшего пересадку костного мозга (ПКМ) в связи с развитием острого миелоидного лейкоза. После ПКМ у пациента в отсутствие приёма нейролептиков значительно ослабла психотическая симптоматика, а также значительно повысился уровень социального функционирования. Два обследования, проведенных через 2 и 4 года после ПКМ, показали устойчивые значительные улучшения как с точки зрения психотических симптомов, так и в плане социального функционирования. В последнее время были осуществлены научные исследования, показавшие, что дисрегуляция иммунной системы является важным патогенным механизмом, связанным с развитием шизофрении. Можно предположить, что ПКМ – клеточная терапия, которая противостоит сбоям, возвращая воспалительные процессы в норму посредством регуляции иммунной системы – может дать положительные результаты у пациентов с резистентной шизофренией. Необходимы дополнительные исследования с целью определения реальной эффективности ПКМ при шизофрении.
История вопроса
Появляются все новые данные, говорящие о корреляции между развитием шизофрении и наличием иммунных отклонений. По данным полногеномных поисков ассоциаций – исследований, направленных на поиск генов, связанных с шизофренией – среди того множества генетических локусов, которые предположительно связаны с развитием болезни, статистический показатель "отношение шансов" зачастую высок у областей, связанных с функционированием иммунной системы. Хотя шизофрения считается синдромом, вызываемым разными биологическими причинами, одним из механизмов, общих для всех случаев заболевания, может быть нарушение работы иммунной системы.
Ассоциация материнских инфекций, протекающих во время беременности, с нарушениями нервно-психического развития у будущего ребенка была выявлена давно, но остается предметом дискуссий. После случившейся в 1964 году пандемии краснухи заболеваемость шизофренией возросла с менее 1 % (в популяции, не подвергшейся эпидемии) до около 20 % (в популяции, подвергшейся воздействию эпидемии) (4). Последовавшие за этим исследования исторических данных по вспышкам заболеваемости гриппом, корью, свинкой, ветрянкой и полиомиелитом выявили наличие ассоциации с развитием шизофрении (5). Вместе с тем наличие ассоциации удалось реплицировать не во всех исследованиях. Причина противоречивости выводов исследователей может крыться в различных подходах к тому, что именно считать "популяцией, подвергшейся действию заболевания". И все же результаты нескольких проспективных исследований с использованием возрастных когорт (7, 8) последовательно продемонстрировали наличие ассоциации между инфекциями во время беременности и психическими заболеваниями у потомства. Более того, список типов патогенов расширился: теперь это и бактерии – в частности, те, что вызывают воспаление легких, синуситы и тонзиллиты – и паразитический протист Toxoplasma gondii (7, 9).
Как может такая разношерстная группа патогенов в одинаковой степени увеличивать риск развития психотических расстройств? Общая черта этих предполагаемых патогенов – то, что они способны провоцировать в организме беременной женщины иммунный ответ, направленный против плода. В пользу этого предположения говорит тот факт, что наибольший риск представляет длительная лихорадка, чья интенсивность превышает некий порог (10). Следовательно, когда активация иммунной системы превышает соответствующий предел – будь то из-за воздействия внешней среды или из-за генетической предрасположенности – повышается и риск заболевания. Действительно, повышенный риск развития шизофрении оказался ассоциирован с целым рядом факторов, каждый из которых приводит к активации иммунных реакций – это и аутоиммунные заболевания при беременности, и аллергии, и астма, и сильный стресс, и воздействие загрязненной окружающей среды (7, 8). В свете этих данных легче понять результаты, полученные недавно двумя группами ученых, осуществивших проспективные исследования. В результате этих проспективных исследований не было обнаружено ассоциации между внутриутробными инфекциями и риском шизофрении – после коррекции результатов с целью учета общего воздействия родительских инфекций, а также психических заболеваний родителей и их социоэкономического статуса (11, 12).
Появляется все больше результатов исследований, свидетельствующих о значительной роли нейровоспалительных процессов и иммунной системы в патофизиологии шизофрении. Во множестве научных статей высказывается поддержка гипотезы, согласно которой активация иммунной системы повышает риск развития шизофрении во взрослом возрасте. Более того, данные, полученные в результате анализов генома и компонентов крови, а также посмертных исследований и прижизненных визуализационных исследований (19) позволяют предположить, что активация иммунной системы связана с патофизиологией шизофрении.
Почти при каждом аутоиммунном заболевании можно добиться благоприятного результата, осуществив иммуноабляцию с последующей пересадкой костного мозга (ПКМ) (20). Исследования с использованием радиационных химер показали, что иммунная и кроветворная система используют один и тот же тип стволовой клетки (20).
Осуществив клинические наблюдения за течением шизофрении после ПКМ, мы можем значительно улучшить наше понимание той роли, которую играет иммунная система при данном заболевании. Sommer и van Bekkum составили призыв к гематологам и психиатрам с просьбой оповещать их о клинических случаях, и разослали этот призыв для публикации в соответствующих научных журналах (20).
В описываемом нами клиническом случае ПКМ оказала значимый терапевтический эффект при резистентной шизофрении с преобладанием бредовой симптоматики и галлюцинаций. Насколько нам известно, это первый случай удачной терапии резистентной шизофрении с помощью ПКМ.
Описание случая
Описываемый пациент – мужчина в возрасте 24 лет. Роды протекали без патологии, пациент развивался нормально. После окончания университета пациент стал служащим корпорации, демонстрировал обычный уровень социальных навыков. Отсутствуют какие-либо сведения о злоупотреблении спиртным или приеме наркотиков, а также об эпилептических припадках. У родственников пациента не было отмечено ни психических расстройств, ни нарушений развития. В возрасте 23 лет у пациента развились бессонница, раздражительность и тревожность. У него также были отмечены возбуждение, несвязная речь, бред преследования и параноидные идеи. Уровень сознания оставался в норме, также не было отмечено судорог. Пациент посещал психиатрическое отделение госпиталя при Университете Симане. Оценка психического статуса пациента подтвердила наличие слуховых галлюцинаций, подозрительности, и таких отклонений, как избегание социальных контактов, бред преследования, снижение уровня социального функционирования. Пациенту был поставлен диагноз "параноидная шизофрения" в соответствии с критериями DSM-IV-TR (21). Физикальное и неврологическое обследование пациента не выявили явных отклонений. Результаты стандартных анализов сыворотки и мочи также были в пределах нормы. Не было выявлено отклонений и в ходе ЭЭГ-, КТ- и МРТ-исследований головного мозга. Пациенту был назначен кветиапин (КТП) в дозировке 300 мг/сут. Через неделю у него сохранялись слуховые галлюцинации, подозрительность, избегание социума, бред преследования и сниженный уровень социального функционирования. Поскольку пациент отказывался принимать нейролептики, за его лекарственной терапией стали следить члены семьи – они удостоверялись в том, что он принимал лекарства. Несмотря на это, было отмечено значительное ухудшение симптоматики. Дополнительно к кветиапину был назначен рисперидон (РИС) (12 мг/сут) и оланзапин (20 мг/сут), однако это нисколько не повлияло на симптомы. Уровень социального функционирования также снизился. Под резистентной шизофренией понимают такую форму заболевания, при которой по меньшей мере две смены антипсихотика не оказывают существенного воздействия на симптомы, причем срок приема каждого препарата должен составлять по меньшей мере 4 недели, препарат должен назначаться в терапевтически адекватной дозе, и хотя бы один из опробуемых препаратов должен быть антипсихотиком второго поколения (22). В соответствии с этими критериями пациенту был поставлен диагноз "резистентная шизофрения" (23).
В возрасте 24 лет у пациента появились жалобы на сильную усталость, нарастающий жар, боли в суставах, кровоточивость дёсен и одышку. Специалисты Гематологического отделения больницы при Университете Симане выявили у пациента острый миелоидный лейкоз. Пациент дал свое согласие на прохождение ПКМ; однако было неочевидно, что он сможет перенести психологический стресс, связанный с ПКМ, особенно со стадией изоляции. Мы осуществили пробную 7-дневную изоляцию пациента. Во время этой изоляции у него сохранялись слуховые галлюцинации, подозрительность и бред преследования, однако не было отмечено серьезного психомоторного возбуждения. Более того, у медицинского персонала не возникало проблем при взаимодействии с пациентом. В результате совещания с гематологами было решено, что пациенту удастся вынести стресс, связанный с изоляцией. В период изоляции в стерильной палате пациент не получал никаких нейролептических средств.
Неделю спустя была осуществлена ПКМ. Пациент был помещен в изоляционную палату асептического отделения на 34 дня. Мы посещали его три раза в неделю на протяжении изоляционной стадии, чтобы оценить его психический статус и определить необходимость дополнительной терапии. Пациент не получал нейролептиков, поскольку отказывался от них; однако его психическое состояние оставалось стабильным. Более того, изоляционная стадия ПКМ прошла без проблем. По завершении ПКМ пациенту был назначен метотрексат и циклоспорин А, чтобы предупредить реакцию "трансплантат против хозяина" (РТПХ). Через три недели после ПКМ у пациента были обнаружены начальные симптомы РТПХ, и циклоспорин А по указанию гематологов был заменен на такролимус.
Через тридцать дней у пациента почти не осталось психотической симптоматики. Он не получал нейролептиков и его психическое состояние не требовало какой-либо иной терапии. Психический статус пациента оценивался с помощью Шкалы оценки позитивных и негативных синдромов (Positive and Negative Syndrome Scale, PANSS) (24). Социальное функционирование оценивалось по шкале оценки глобального функционирования (GAF) в соответствии с DSM-IV-TR (21). Получаемое пациентом лечение и течение его болезни отражены на Рис. 1. В 2017 году, через 8 лет после ПКМ, соматическое и психическое состояние пациента продолжают улучшаться, он чувствует себя очень хорошо и не демонстрирует каких-либо остаточных психиатрических симптомов. Более того, радикально повысился уровень его социального функционирования, и он продолжает работать в известной компании.
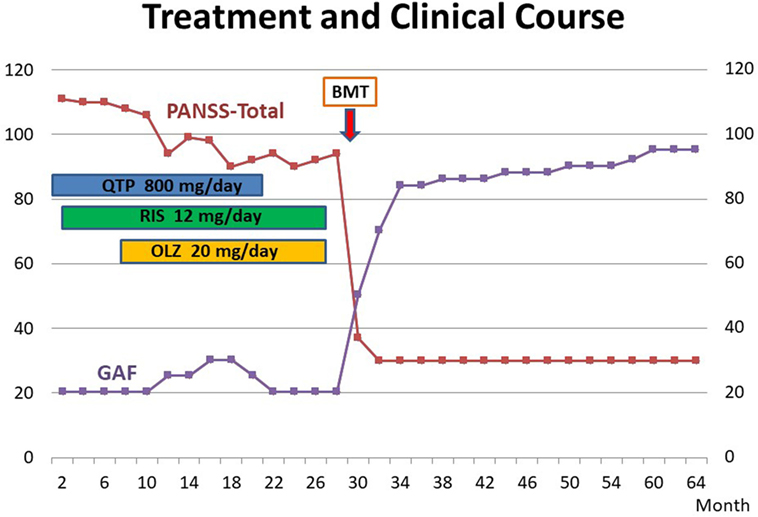
Рисунок 1. Терапия и течение болезни. Оценка психической симптоматики проводилась с использованием шкалы PANSS (24). Функционирование оценивалось по шкале GAF в соответствии с DSM-IV-TR (21). BMT – пересадка костного мозга; QTP – кветиапин; RIS – рисперидон; OLZ – оланзапин; PANSS - Шкала оценки позитивных и негативных синдромов; GAF - шкала оценки глобального функционирования.
Обсуждение
Пересадка костного мозга может оказаться эффективным способом терапии острых и резистентных форм шизофрении с преобладанием бреда и галлюцинаций. Во время ремиссии психоза наш пациент не подвергался воздействию каких-либо ассоциированных с ПКМ инфекций. Насколько нам известно, это первый случай удачной терапии резистентной шизофрении с помощью ПКМ. С другой стороны, мы не можем исключить вероятности спонтанного улучшения состояния в отсутствие всякой терапии, парадоксального улучшения после отмены нейролептиков, а также лечебного эффекта от приёма нескольких иммуномодулирующих препаратов.
Мы, конечно же, не можем утверждать об иммунном характере патогенеза шизофрении на основании одного клинического случая. Однако, поскольку гипотеза о роли иммунной системы в патогенезе шизофрении нашла поддержку в нескольких научных публикациях (25, 26), мы полагаем, что и врачи, осуществляющие ПКМ, и их пациенты должны учитывать возможность успешной терапии шизофрении данным методом.
В исследовании с использованием потомства самок мышей, подвергшихся активации иммунной системы при беременности (MIA offspring), Hsiao et al. выявили отклонения в функционировании иммунной системы у данных животных, которых используют для моделирования аутизма и шизофрении (27). Эффект материнской иммунной активации (МИА) у беременных грызунов достигается путем введения животным полирибоинозитиловой-полирибоцитидиловой кислоты (Poly I:C), что приводит к стойким отклонениям в иммунной системе и в поведении потомства (9, 27-30). Более того, сообщалось о том, что МИА, индуцированная с помощью Poly I:C, приводит к возникновению стойкой гиперчувствительности CD4+ Т-лимфоцитов, а также к гиперчувствительной иммунной системе у потомства. Также сообщалось, что поведенческие отклонения у грызунов можно отчасти скорректировать с помощью ПКМ (27).
Данные нашей публикации можно поставить в ряд с несколькими исследованиями с использованием животных моделей, в которых ПКМ показала эффективность в коррекции симптомов неврологических заболеваний (31-33). Derecki et al. определили, что происходящая благодаря ПКМ нормализация работы микроглии даёт вклад в коррекцию поведенческих отклонений в мышиной модели синдрома Ретта. Полученные результаты говорят о том, что ПКМ корректирует нарушения микроглиальной функции в мозге. Судя по всему, патологические отклонения в микроглиальных клетках мозга являются одним из важных неврологических факторов при шизофрении (34, 35). С другой стороны, если фокусировать внимание лишь на микроглии, трудно описать тот механизм, посредством которого ПКМ смогла вдруг обратить вспять ход болезни в описываемом нами случае.
Sommer et al. опубликовали клинический случай пациента, у которого развился тяжелый психоз после ПКМ от донора, страдавшего шизофренией (36). Эту публикацию можно также рассматривать как свидетельство в поддержку возможной эффективности ПКМ при шизофрении (37).
Очевидна необходимость проведения дополнительных исследований с большим количеством участников, поскольку на данный момент остается совершенно непонятным, как ПКМ ассоциирована с изменениями состояния при шизофрении, и как ПКМ воздействует на центральную нервную систему.
Заключительные замечания
В случае с нашим пациентом, ПКМ оказалась эффективным средством терапии острой резистентной шизофрении с преобладанием бредовой симптоматики и галлюцинаций. Во время ремиссии психоза наш пациент не подвергался воздействию каких-либо ассоциированных с ПКМ инфекций. Конечно же, мы не можем утверждать об иммунном характере патогенеза шизофрении на основании одного клинического случая. Однако гипотеза о том, что дисфункция иммунной системы является одним из ключевых элементов в патогенезе шизофрении, получила поддержку в нескольких научных публикациях (26), и мы считаем, что как врачи, осуществляющие ПКМ, так и их пациенты должны учитывать возможность эффективной терапии резистентной шизофрении с помощью данного метода. Вероятно, ПКМ не представляет собой универсального лекарства, подходящего для каждого пациента с шизофренией, но этот метод терапии определенно обладает потенциалом к снижению тяжести заболевания и улучшению качества жизни. Описанный нами клинический случай является предварительной демонстрацией безопасности и эффективности ПКМ при резистентной шизофрении. Несомненно, необходимо провести исследования с большим количеством участников, поскольку на данный момент остается совершенно непонятным, как ПКМ ассоциирована с изменениями состояния при шизофрении и как ПКМ воздействует на центральную нервную систему.
Оригинальная статья на английском: Remission of Psychosis in Treatment-Resistant Schizophrenia following Bone Marrow Transplantation: A Case Report (Front. Psychiatry, 21 September 2017)
Авторы: Tsuyoshi Miyaoka*, Rei Wake, Sadayuki Hashioka, Maiko Hayashida, Arata Oh-Nishi, Ilhamuddin Abdul Azis, Muneto Izuhara, Keiko Tsuchie, Tomoko Araki, Ryosuke Arauchi, Rostia Arianna Abdullah, Jun Horiguchi
См. также: Трансплантация костного мозга у пациентов с шизофренией: призыв к публикации клинических случаев
Перевод : Тимеев Артём Геннадьевич (переводы фармакологических, биотехнологических текстов с русского на английский и с английского на русский; email: Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра.)